Железо и соляная кислота – это два химических вещества, которые вступают во взаимодействие между собой. Эта реакция может проходить за определенных условий и обладает некоторыми особенностями. Понимание того, как протекает эта реакция, позволяет лучше понять механизм химических процессов и их влияние на окружающую среду.
Когда железо и соляная кислота смешиваются, происходит химическое взаимодействие. Образуются газы, которые могут быть видимыми или невидимыми, в зависимости от концентрации реагентов и условий проведения эксперимента. Одним из главных продуктов реакции является водород, который образуется в результате диссоциации соляной кислоты и взаимодействия с железом.
Особенностью реакции железа с соляной кислотой является ее эффект на окружающую среду. Во-первых, взаимодействие этих веществ может сопровождаться выделением тепла, что может привести к изменению температуры среды. Во-вторых, образующиеся газы могут быть опасными, особенно при выполнении эксперимента в неподходящих условиях. Это может потребовать соблюдения особых мер предосторожности для сохранности и здоровья.
Условия реакции железа с соляной кислотой

Первое и самое важное условие - наличие реагентов. Для реакции необходимы железо и соляная кислота. Железо может быть представлено в различных формах, например, в виде гвоздей или стружки, а соляная кислота - в виде жидкости соответствующей концентрации.
Второе условие - контакт между железом и соляной кислотой. Для этого необходимо поместить железо в соляную кислоту или добавить соляную кислоту к железу. Контакт позволяет начать химическую реакцию между реагентами.
Третье условие - наличие катализатора. Железо является катализатором данной реакции, то есть оно ускоряет протекание реакции и увеличивает его эффективность.
Важно отметить, что при протекании данной реакции выделяется водородный газ, поэтому следует обеспечить правильные условия безопасности, такие как проведение реакции в хорошо проветриваемом помещении или использование специальных систем отвода газов.
Итак, для успешного протекания реакции железа с соляной кислотой необходимо выполнение трех основных условий: наличие реагентов, контакт между железом и соляной кислотой, а также наличие катализатора в виде железа.
Реакционная система и реактивы
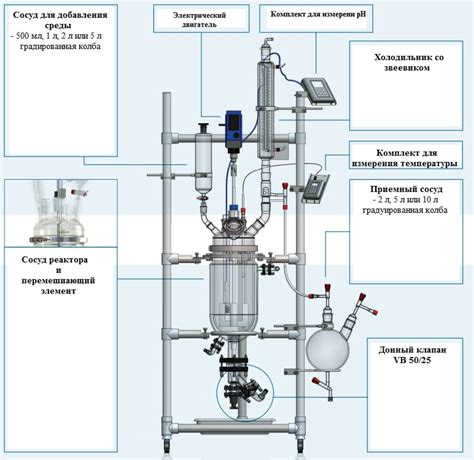
Реакционная система
В реакции железа с соляной кислотой реакционная система состоит из двух основных компонентов - железа (Fe) и соляной кислоты (HCl). Железо является активным металлом, а соляная кислота - сильной минеральной кислотой. Вместе они образуют энергетически выгодную реакцию.
Реактивы
Железо (Fe)
Железо - металл, который легко окисляется. В реакции с соляной кислотой железо выступает в качестве источника электронов для окисления. Обычно используются фольга из чистого железа или кусочки железа, которые при реакции полностью растворяются в соляной кислоте.
Соляная кислота (HCl)
Соляная кислота - химическое соединение, образованное из воды (H2O) и хлористого водорода (HCl). В реакции она выступает в качестве окислителя, принимает электроны от железа и образует хлорид железа (FeCl2). Соляная кислота является крепкой кислотой, что означает ее высокую активность и способность эффективно реагировать с другими веществами.
Температурный режим и давление
Реакция железа с соляной кислотой протекает при обычных температурных условиях. Однако температура среды может влиять на скорость протекания реакции.
При повышении температуры соляной кислоты увеличивается активность ее молекул, что способствует более интенсивному протеканию реакции. Также повышение температуры может привести к увеличению скорости диффузии железа к поверхности кислоты, что также ускоряет реакцию.
Однако при слишком высоких температурах может происходить разложение соляной кислоты, что может затруднить протекание реакции и изменить ход процесса.
Давление также может оказывать влияние на реакцию железа с соляной кислотой. Увеличение давления может способствовать увеличению контактной поверхности между кислотой и железом, что повышает скорость реакции. Однако при слишком высоких давлениях могут возникнуть и другие факторы, такие как растворение побочных веществ или изменение условий реакции, что может изменить ход процесса.
Таким образом, температурный режим и давление могут оказывать существенное влияние на протекание реакции железа с соляной кислотой, изменяя скорость и условия процесса.
Протекание реакции железа с соляной кислотой

При протекании данной реакции образуются ион железа(II) и хлороводород, выделяющийся в виде газа. Реакция происходит следующим образом:
Fe + 2HCl → FeCl2 + H2
Реакция протекает быстро и выделяет значительное количество тепла. При этом железо растворяется и образует ионы железа(II), а соляная кислота распадается на ионы водорода и хлора.
Одной из особых особенностей данной реакции является коррозия и разрушение железных предметов, подвергшихся воздействию соляной кислоты. Коррозия железа происходит из-за образования хлорида железа(II), который является сильным окислителем и способствует разрушению металла.
Для успешного протекания реакции необходимы определенные условия, такие как наличие достаточной концентрации соляной кислоты и контакт между металлом железа и кислотой. Также реакция протекает с большей скоростью при повышенной температуре.
Реакция железа с соляной кислотой находит широкое применение в различных отраслях промышленности, таких как производство хлорида железа(II), очистка и сушка газов, а также в лабораторной практике для получения и применения соответствующих продуктов реакции.
Стадии реакции

Реакция железа с соляной кислотой проходит через несколько стадий. Зависимость скорости реакции от концентрации реагентов указывает на поэтапность процесса.
Первой стадией является диссоциация соляной кислоты. Водородные ионы и ионы хлора образуются в растворе, и на этой стадии еще не происходит непосредственной реакции с железом.
Далее происходит адсорбция железа на поверхности водородных ионов. Эта стадия называется адсорбцией железа. На поверхности железа образуется пленка Fe(H2O)6²⁺, которая является активным участником реакции.
Третьей стадией является протекание химической реакции между адсорбированным железом и ионами хлора. Образуются ионы железа(II), при этом выделяется газовый продукт - водород. Количество выделяемого водорода напрямую зависит от концентрации ионов хлора и железа.
Образование продуктов реакции

Использование катализаторов

В данной реакции железо является катализатором, поскольку оно не растворяется и не изменяется в процессе протекания реакции. Катализатор железа значительно сокращает время, необходимое для протекания реакции между железом и соляной кислотой.
Использование катализатора в реакции между железом и соляной кислотой позволяет значительно увеличить скорость реакции без изменения исходных веществ. Катализаторы могут быть использованы для более эффективного протекания процессов, что делает их важными компонентами в различных химических процессах.