Молярная масса водорода – это величина, которая показывает массу одного моля водорода. Определение молярной массы вещества является важным шагом при проведении химических расчетов и позволяет установить соотношение между массой и количеством вещества. В данной статье мы рассмотрим несколько методов и формул, с помощью которых можно определить молярную массу водорода.
Первый метод, который можно использовать для определения молярной массы водорода, основан на экспериментальных данных. Для этого необходимо знать массу образца водорода и количество молей, содержащихся в данном образце. После измерения массы и количества молей водорода можно просто разделить массу на количество молей и получить искомую величину.
Второй метод основан на использовании химических формул и изотопов водорода. Водород состоит из трех изотопов: протия, дейтерия и трития. Каждый из этих изотопов имеет разную массу, и для определения молярной массы водорода необходимо учитывать их соотношение. С помощью специальных формул и таблиц изотопного состава можно рассчитать среднюю молярную массу водорода.
Определение молярной массы водорода

Молярная масса водорода определяется как масса одного моля водорода. Так как атомный номер водорода равен 1, молярная масса его атома составляет примерно 1 г/моль.
Для определения молярной массы водорода можно использовать различные методы и формулы.
- Метод вычисления по изотопам:
Водород имеет три изотопа: протий, дейтерий и тритий. Их относительные атомные массы составляют соответственно около 1, 2 и 3. Для расчета молярной массы водорода можно использовать среднюю массу изотопов, учитывая их относительные содержания в природе.
- Метод вычисления по химическим соединениям:
Водород встречается в различных химических соединениях, таких как вода, метан, аммиак и др. Молярная масса водорода в этих соединениях может быть найдена путем вычисления средней массы на основе массы атома водорода и количества его атомов в каждом соединении.
Определение молярной массы водорода имеет важное значение в химии, так как это позволяет проводить расчеты, связанные с количеством вещества и реакционной стехиометрией. Точное значение молярной массы водорода позволяет более точно определять массу других веществ и проводить аналитические расчеты.
Роль молярной массы в химии
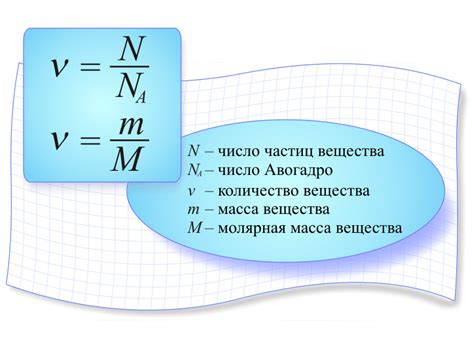
Знание молярной массы позволяет проводить расчеты количества вещества в реакции, а также определять соотношения между различными веществами. Например, зная молярную массу вещества, можно определить массу определенного количества вещества по формуле:
масса = молярная масса × количество вещества
Молярная масса также важна при проведении расчетов по закону сохранения массы и сохранению атомных ионов внутри реакции. Она используется для определения состава химических соединений и расчетов концентрации растворов.
Для определения молярной массы вещества можно использовать различные методы, такие как химический анализ, масс-спектрометрию и определение относительной атомной массы атомов в элементе. Знание молярной массы позволяет более точно проводить химические расчеты и предсказывать результаты химических реакций.
Формула расчета молярной массы водорода
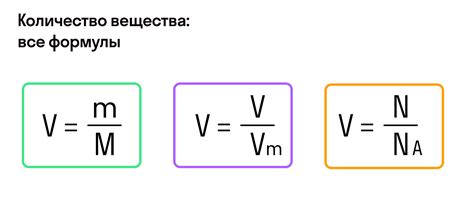
молярная масса водорода (H) = масса водорода (H) / количество водорода (H)
Для определения массы водорода используйте весы, чтобы точно измерить массу пробы водорода. Количество водорода можно определить, зная число молекул водорода в пробе или зная ее стехиометрию.
Стехиометрический коэффициент для водорода в простейшем соединении, молекулярном водороде (H2), равен 2. Это означает, что в каждой молекуле водорода содержится 2 атома водорода. Таким образом, количество водорода всегда будет равно половине числа молекул водорода.
Используя данную информацию, формула для расчета молярной массы водорода (H2) можно записать следующим образом:
- Суммарная масса образцов водорода (H2): вес1 + вес2 + вес3 + ...
- Общее количество водорода (H2): (количество1 + количество2 + количество3 + ...) / 2
Подставьте соответствующие значения в формулу и рассчитайте молярную массу водорода (H2). Полученное значение будет выражено в г/моль.
Методы определения молярной массы водорода
- Метод сравнения: основан на сравнении массы водорода с массой других известных веществ. Для этого измеряют массу водорода, а затем сравнивают с массой известного вещества, например, кислорода или азота. Известная масса вещества делится на количество вещества, что позволяет определить молярную массу водорода.
- Метод газовых законов: применяется при измерении физических свойств водорода, таких как давление, объем и температура. С использованием уравнения состояния идеального газа (PV = nRT), можно определить количество вещества (n) исходя из известных значений давления (P), объема (V), температуры (T) и газовой постоянной (R). Зная количество вещества, можно определить молярную массу водорода.
- Метод электролиза: основан на разложении воды на водород и кислород под воздействием электрического тока. При известной силе тока и времени электролиза можно определить количество вещества водорода, что позволяет найти молярную массу водорода.
- Метод массового спектрометра: использует способность массового спектрометра разделить ионизированные атомы водорода по их массе. По результатам спектрального анализа можно определить отношение массы и заряда ионов водорода, что позволяет вычислить молярную массу водорода.
В зависимости от условий эксперимента и доступного оборудования можно выбрать один из указанных методов для определения молярной массы водорода. Комбинация различных методов может также быть использована для повышения точности результатов.
Использование осмотического давления

Для определения молярной массы водорода с помощью осмотического давления требуется специальная аппаратура, называемая осмометром. Этот прибор позволяет измерить осмотическое давление раствора, а затем, используя закон физической химии, можно вычислить молярную массу вещества.
Процесс определения молярной массы водорода с помощью осмотического давления основан на сравнении осмотического давления растворов водорода с давлением чистой воды. Для этого водород газ перекачивается через полупроницаемую мембрану в воду, и измеряется разница в осмотическом давлении обеих растворов. Исходя из измеренных значений и используя формулы, можно определить молярную массу водорода.
Метод осмотического давления широко применяется в химии и физике для определения молярной массы различных веществ, включая водород. Однако, для точных результатов требуется использование высокоточного оборудования и аккуратные эксперименты.
Использование метода газового диффузии
Процесс газовой диффузии заключается в том, что молекулы газа распространяются через пространство, заполненное другим газом, под воздействием их теплового движения. Скорость диффузии зависит от массы молекулы газа и от состояния газа (температура, давление и так далее).
Для определения молярной массы водорода методом газового диффузии можно использовать закон Грэма. Согласно этому закону, скорость диффузии обратно пропорциональна квадратному корню из молярной массы газа. Таким образом, если известна скорость диффузии водорода и другого газа, можно использовать формулу для определения молярной массы водорода:
MH = Mg * (vg/vH)2
Где MH – молярная масса водорода, Mg – молярная масса другого газа, vg – скорость диффузии другого газа, vH – скорость диффузии водорода.
Для проведения эксперимента по определению молярной массы водорода методом газового диффузии необходимо иметь знание о законе Грэма и его применимости к конкретной ситуации. Также необходимо обладать средствами для измерения скорости диффузии и знанием о свойствах газов, которые будут использоваться в эксперименте.
Использование электролиза

Для определения молярной массы водорода методом электролиза можно использовать следующий эксперимент:
- Подготовьте аппарат для электролиза, состоящий из двух электродов - катода и анода.
- Наполните электролитическую ячейку раствором воды и добавьте к нему немного серной кислоты для улучшения проводимости.
- Поместите электроды в раствор таким образом, чтобы они не касались друг друга.
- Подключите источник постоянного тока к электродам.
- В процессе электролиза вода начнет разлагаться на кислород и водород в соотношении 2:1.
- Водород будет откладываться на катоде, а кислород - на аноде.
- Измерьте массу водорода, собранного за определенное время.
- Используя полученные данные, можно вычислить количество вещества водорода и, следовательно, его молярную массу.
Определение молярной массы водорода методом электролиза позволяет получить точный и надежный результат. Однако для проведения данного эксперимента необходимо обладать определенными знаниями в области электрохимии и обеспечить все необходимые условия для проведения электролиза.
Определение молярной массы водорода на практике

Один из таких методов основан на использовании закона Дальтона. Этот закон гласит, что смесь газов, состоящая из разных компонентов, имеет суммарное давление, равное сумме давлений каждого компонента в отдельности. С помощью этого закона можно определить молярную массу водорода.
Для проведения эксперимента, необходимо иметь ампулу с известным объемом, содержащую известное количество водорода. Заполнив ампулу водородом, при комнатной температуре и давлении, измеряют ее массу. Затем, с помощью газового сборщика, ампулу медленно нагревают до определенной температуры. При этом, водород начинает выделяться из ампулы. Масса ампулы, после остывания, снова измеряется.
Зная изначальную массу ампулы с водородом и массу ампулы после выделения водорода, можно определить массу выделившегося водорода. Далее, используя закон Дальтона, можно рассчитать количество молекул водорода и вычислить его молярную массу.
Примечание: При проведении данного эксперимента необходимо соблюдать все меры предосторожности, ведь водород является легковоспламеняющимся газом.
Применение молярной массы водорода в химических расчетах

Одним из основных способов применение молярной массы водорода является расчет количества вещества водорода по массе и наоборот. Для этого используется формула:
n = m/M
где n - количество вещества в молях, m - масса водорода, M - молярная масса водорода.
Также молярная масса водорода используется для расчета объема газовых реакций. Для этого применяется формула:
V = n*Vm
где V - объем газовой реакции, n - количество вещества в молях, Vm - молярный объем вещества.
Правильное определение молярной массы водорода позволяет также проводить расчеты по стехиометрии химических реакций. Например, для определения массового соотношения в веществах, участвующих в реакции, можно использовать формулу:
m1/M1 = m2/M2
где m1 и m2 - массы веществ, участвующих в реакции, M1 и M2 - их молярные массы соответственно.
Таким образом, знание молярной массы водорода полезно для проведения различных химических расчетов и позволяет более точно определить количественные характеристики вещества.