Вещества, с которыми мы сталкиваемся в повседневной жизни, могут быть разнообразными по своей природе. Некоторые из них являются простыми веществами, состоящими из одного элемента, таких как кислород или сера. Другие - сложные вещества, состоящие из разных элементов, таких как вода или сахар. Но возникает вопрос: можно ли разделить эти вещества на отдельные молекулы?
Ответ на этот вопрос зависит от типа вещества. Простые вещества могут быть разделены на отдельные молекулы путем химических реакций или физического разложения. Например, молекулы кислорода можно получить путем разложения молекул воды. Также возможно разделение молекул серы на отдельные атомы, что практически используется в промышленности.
Сложные вещества, такие как вода или сахар, состоят из многочисленных молекул, связанных вместе в определенном порядке. Разделение этих веществ на отдельные молекулы может быть более сложным процессом. Однако, с помощью химических методов, таких как гидролиз или ферментация, возможно разорвать связи между молекулами и получить отдельные молекулы веществ.
Таким образом, ответ на вопрос "Можно ли разделить на отдельные молекулы вещества?" зависит от типа вещества и методов разделения, которые доступны для данного вещества. В некоторых случаях разделение на отдельные молекулы возможно, в других - может требоваться более сложный подход. Однако, современная наука и технологии предоставляют нам возможность изучать и разделять различные вещества на молекулярном уровне, что открывает новые перспективы и применения в различных областях жизни.
Вещества: можно ли разделить на отдельные молекулы?

Некоторые вещества, например, простые молекулярные соединения, можно легко разделить на отдельные молекулы. Примером такого вещества является вода (H2O). Каждая молекула воды состоит из двух атомов водорода (H) и одного атома кислорода (O). Если мы разобьем молекулу воды, мы получим отдельные молекулы водорода и кислорода.
Однако, есть и вещества, которые нельзя разделить на отдельные молекулы без нарушения их структуры. Например, соль (NaCl), состоящая из натрия (Na) и хлора (Cl). В молекуле соли атомы натрия и хлора тесно связаны между собой. Попытка разделить эти атомы приведет к образованию ионов натрия и хлора, что изменит химическую природу вещества.
Таким образом, ответ на вопрос о разделении веществ на отдельные молекулы зависит от их химической структуры и взаимодействия атомов. Некоторые вещества можно разделить на отдельные молекулы без изменения их состава, в то время как другие вещества сохранят свои свойства только при сохранении структуры и взаимодействия их атомов.
Структура веществ

Вещества состоят из атомов, которые объединяются в молекулы. Молекулы, в свою очередь, могут состоять из одного или нескольких атомов одного или различных элементов.
Например, молекула воды (H2O) состоит из двух атомов водорода и одного атома кислорода. Атомы водорода и кислорода, в свою очередь, состоят из еще более мелких частиц - протонов, нейтронов и электронов.
Однако не все вещества могут быть разделены на отдельные молекулы. Некоторые вещества, такие как ионы или полимеры, могут состоять из большого числа атомов, которые объединены в сложные структуры.
Знание структуры веществ позволяет понять и объяснить их свойства и поведение, а также разрабатывать новые материалы с нужными характеристиками.
Молекулы или атомы веществ?

Атомы - это основные строительные блоки всей материи. Они являются наименьшими единицами вещества, которые сохраняют его химические свойства. Атомы объединяются в молекулы, образуя различные вещества. Некоторые вещества состоят из одного вида атомов - это простые вещества, например, кислород или железо. Другие вещества состоят из различных видов атомов, снабжая их разнообразными химическими свойствами.
Молекулы - это группы двух или более атомов, связанных друг с другом. Молекулярная структура определяет химические свойства вещества. Молекулы могут быть одинаковыми (например, молекула O2 - два атома кислорода) или разными (например, молекула H2O - два атома водорода и один атом кислорода).
Таким образом, можно сказать, что вещество состоит из молекул, которые в свою очередь состоят из атомов. Химические реакции происходят на уровне молекул, когда атомы вступают во взаимодействие, образуя новые молекулы или разрушая старые. Молекулы и атомы - это взаимосвязанные компоненты вещества и обуславливают его свойства и поведение.
Химические и физические методы разделения

В химии и физике существует множество методов разделения вещества на отдельные молекулы. Эти методы позволяют проводить анализ и изучение свойств различных веществ, определять их состав и характеристики.
Одним из самых распространенных методов разделения является хроматография. Этот метод основан на различной способности вещества перемещаться вдоль носителя под воздействием различных физических или химических процессов. Хроматография широко применяется в различных областях, включая химию, биологию и фармакологию.
| Метод | Описание |
|---|---|
| Дистилляция | Метод разделения жидкостей на основе различия в температуре их кипения. |
| Экстракция | Метод разделения веществ на основе различия их растворимости в различных растворителях. |
| Фильтрация | Метод разделения смесей на основе различия размеров частиц вещества. |
| Ионный обмен | Метод разделения веществ на основе различия зарядов ионов. |
Кроме того, существуют и другие методы разделения, такие как испарение, сублимация, фракционирование и электрофорез. Каждый из них отличается своими принципами и применяется в зависимости от задачи и свойств вещества.
Химические и физические методы разделения являются неотъемлемой частью научного исследования и производственных процессов. Они позволяют проводить более точные измерения и получать более точные результаты, что открывает новые возможности для развития науки и технологии.
Химическая реакция как способ разделения

При химической реакции происходит изменение химических связей между атомами в молекулах вещества. Реагенты, участвующие в реакции, претерпевают химические изменения и формируют новые вещества - продукты реакции.
Химическая реакция может быть использована для разделения смесей веществ. Например, при нагревании смеси металлов с кислородом происходит окисление металла и образуется соответствующий оксид, который можно разделить от остальных веществ и получить чистый металл. Также можно использовать химическую реакцию для разделения солей или органических соединений на компоненты.
Одной из важнейших химических реакций, используемых в промышленности и научных исследованиях, является реакция гидролиза. При гидролизе молекула вещества разлагается на две или более других вещества под действием воды. Это позволяет изучать состав и свойства веществ, а также получать новые соединения.
Химическая реакция представляет собой мощный инструмент для разделения веществ и получения новых соединений. Она играет важную роль в химической промышленности, научных исследованиях и повседневной жизни людей.
Деструкция веществ: возможно ли полное разложение?
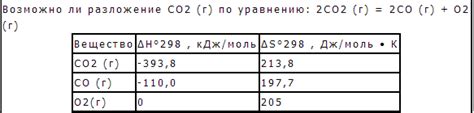
При разложении вещества на отдельные молекулы обычно используются химические реакции, такие как гидролиз, окисление, восстановление и другие. Однако, не все вещества могут быть полностью разложены на отдельные молекулы.
Некоторые вещества могут образовывать макромолекулы, такие как полимеры, которые состоят из множества связанных между собой молекул. В таком случае, разложение таких веществ на отдельные молекулы может быть затруднено или невозможно.
Также существуют вещества, которые образуют ансамбли молекул, такие как кристаллы. Кристаллическая решетка кристаллического вещества представляет собой упорядоченную структуру, где молекулы прочно связаны между собой. Разложение таких веществ на отдельные молекулы может требовать сложных и специфических условий.
Большинство обычных веществ, таких как вода, соли, кислоты и основания, могут быть полностью разложены на отдельные молекулы при определенных условиях.
| Вещество | Возможность полного разложения |
|---|---|
| Вода | Да |
| Соляная кислота | Да |
| Содержащийся в организмах белок | Нет |
Применение разделения на отдельные молекулы

Возможность разделить вещество на отдельные молекулы имеет важное значение в различных областях науки и промышленности.
В химии разделение на отдельные молекулы помогает устанавливать химический состав вещества и изучать его свойства. Путем анализа молекулярной структуры можно определить, какие химические элементы присутствуют в веществе и как они соединены между собой. Это позволяет улучшить процессы синтеза химических соединений, создавать новые материалы и прогнозировать их свойства.
В фармацевтической промышленности разделение на отдельные молекулы используется для изучения структуры и действия лекарственных веществ. Это позволяет разрабатывать более эффективные и безопасные препараты, а также находить новые способы лечения различных заболеваний.
В биологии разделение на отдельные молекулы помогает изучать молекулярные механизмы жизнедеятельности организмов. Изучение структуры и функции биомолекул, таких как ДНК, РНК, белки, позволяет лучше понять принципы наследственности, механизмы болезней и развитие организмов.
В промышленности разделение на отдельные молекулы применяется в различных процессах производства. Например, в пищевой промышленности это позволяет получать и очищать различные продукты, такие как сахар, растительные и животные масла, спирт. В электронной промышленности разделение на отдельные молекулы помогает создавать и очищать материалы для производства полупроводников и электронных компонентов.
Таким образом, разделение на отдельные молекулы играет важную роль в научных и технических исследованиях, дает возможность улучшать существующие процессы, разрабатывать новые продукты и материалы, а также повышать эффективность различных технологических процессов.