Аммиак – один из наиболее важных промышленных химических соединений, широко используемый в различных отраслях промышленности. С его помощью производят удобрения, пластик, красители, взрывчатые вещества и многое другое. Однако процесс получения аммиака является сложным и требует особых знаний и навыков.
Одним из методов получения аммиака является вытеснение воды. В основе этого метода лежит реакция между аммиаком и водой, при которой формируется аммиачная соль и выделяется тепло. Суть этого метода заключается в том, чтобы произвести реакцию, а затем отделить аммиачную соль от полученной смеси. Для этого используют различные способы, включая дистилляцию и фильтрацию.
Преимуществом метода вытеснения воды является его относительная простота и доступность. Он может быть использован как в лабораторных условиях, так и в промышленных масштабах, что делает его универсальным и удобным для производства аммиака. Однако важно помнить, что процесс получения аммиака является опасным и требует соблюдения всех необходимых мер безопасности.
Методы получения аммиака без использования загрязняющих веществ
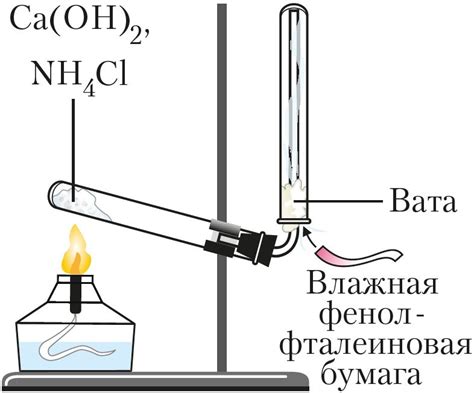
В процессе получения аммиака многие методы включают использование загрязняющих веществ, таких как аммиачная селитра или аммиачная соль. Однако существуют также методы, которые позволяют получать аммиак без участия таких загрязняющих веществ.
Один из таких методов - это метод прерывного получения аммиака. В этом методе используется нагревание смеси газов, содержащих азот и воду, в присутствии катализатора. При этом происходит разложение воды на аммиак и кислород. Аммиак выделяется в газовой фазе, в то время как кислород и другие газы остаются в остатке смеси.
Еще один метод получения аммиака без использования загрязняющих веществ - это метод электролиза воды. При этом методе вода разлагается на молекулы водорода и кислорода с помощью электрического тока. Полученный водород затем реагирует с азотом, образуя аммиак.
Таким образом, существуют методы получения аммиака без использования загрязняющих веществ, которые могут быть полезными в областях, где необходимо минимизировать воздействие на окружающую среду и сократить выбросы загрязняющих веществ.
Использование метода Габера

Процесс получения аммиака по методу Габера осуществляется в несколько этапов. Сначала аммиак получают путем нагревания аммиака и воды в реакторе под давлением. Затем образовавшийся пар аммиака и воды захватывается и конденсируется в специальном испарителе. Отделение аммиака от воды осуществляется путем дальнейшего нагревания полученного раствора аммиака, что приводит к испарению аммиака. Испаренный аммиак затем захватывается и конденсируется, после чего полученный продукт можно собрать и использовать в различных промышленных процессах.
Метод Габера имеет широкое применение в химической промышленности. Аммиак, полученный этим методом, может использоваться в производстве удобрений, кислорода, ацетона, красителей и ряда других продуктов. Более того, аммиак является важным промежуточным продуктом в производстве пластмасс, лекарственных препаратов и многих других химических соединений.
Применение метода Габера-Боша

Преимуществом метода Габера-Боша является его высокая эффективность и экономичность. Он позволяет получать аммиак в больших количествах и с высокой степенью чистоты. Кроме того, процесс осуществляется при относительно низких температурах и давлениях, что снижает энергозатраты.
Основной реакцией, происходящей в ходе метода Габера-Боша, является синтез аммиака по следующему уравнению:
3H2 + N2 → 2NH3
Для проведения реакции необходим специальный катализатор, обычно это железо на активном основе, покрытое оксидами алюминия и калия.
Полученный аммиак имеет широкое применение в промышленности. Он является основным сырьем для производства азотных удобрений, которые являются неотъемлемой частью сельского хозяйства. Аммиак также используется в химической промышленности для получения различных органических соединений, катализаторов и других продуктов.
Получение аммиака из аммиачной соли

Аммиачная соль, также известная как аммиум хлорид (NH4Cl), представляет собой белый кристаллический порошок, который легко растворяется в воде. Для получения аммиака из аммиачной соли необходимо провести термическое разложение соли.
Процесс получения аммиака из аммиачной соли осуществляется следующим образом:
- Взвесьте определенное количество аммиачной соли.
- Поместите аммиачную соль в специальную аппаратуру с нагревательным элементом.
- Включите нагревательный элемент и нагрейте аммиачную соль.
- В результате нагревания аммиачная соль разлагается на аммиак и соляную кислоту.
- Аммиак выпускается в газообразном состоянии и может быть собран и использован в дальнейшем.
- Соляная кислота остается в реакционной смеси и может быть использована в других процессах.
Полученный аммиак можно использовать в различных областях, таких как производство удобрений, производство пищевых добавок, очистка воды и многие другие. Аммиак также может служить сырьем для производства других химических соединений.
Получение аммиака из аммиачной соли является одним из простых и доступных методов получения этого важного вещества. Этот процесс может быть осуществлен в лаборатории или в промышленных масштабах.
Использование метода сухого нагревания
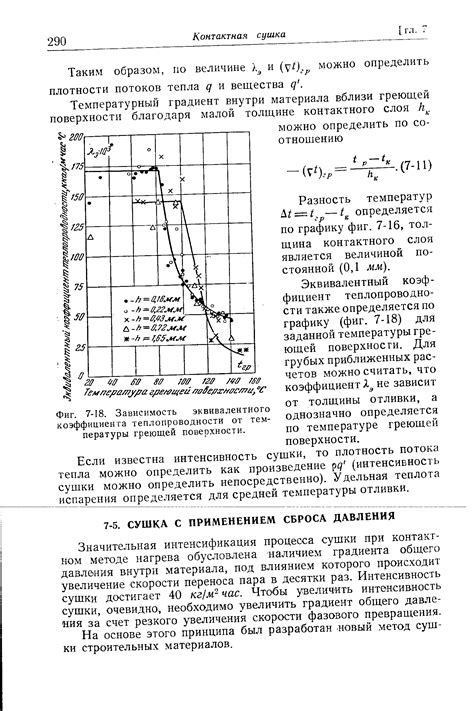
Процесс начинается с подготовки реакционной смеси, которая состоит из аммиака и воды. Обычно используется аммиак с содержанием от 25% до 30% и вода. Смесь нагревается до определенной температуры, при которой аммиак начинает переходить в газообразное состояние и образовывать пары. В процессе нагревания вода начинает испаряться, а аммиак остается в жидком состоянии.
Для конденсации паров аммиака используется специальное оборудование, например, конденсаторы или холодильные машины. Вещество конденсируется и собирается в специальных емкостях. Полученный аммиак можно использовать в различных отраслях промышленности, например, для производства удобрений, химической продукции и др.
Метод сухого нагревания имеет свои преимущества и недостатки. Он отличается высокой эффективностью, позволяет получать аммиак большой чистоты и является экономически выгодным. Однако, требует специального оборудования и контроля процесса нагревания. Также, необходима скрупулезная очистка и обработка полученного аммиака для устранения примесей и повышения качества продукта.
Применение метода электрохимического разложения

Применение метода электрохимического разложения позволяет получить аммиак в высокой концентрации и чистоте. Это особенно важно при использовании аммиака в процессах химической промышленности, таких как производство удобрений, пластических масс, взрывчатых веществ и других продуктов.
Кроме того, метод электрохимического разложения может быть использован для получения аммиака в лабораторных условиях, а также в процессах очистки отработанных газов от азотно-оксидных соединений, что имеет большое значение для охраны окружающей среды и устойчивого развития.
Преимущества метода электрохимического разложения:
- Высокая эффективность и экономичность процесса получения аммиака;
- Высокая степень чистоты и концентрации получаемого аммиака;
- Возможность регулирования скорости и интенсивности процесса разложения;
- Минимальное воздействие на окружающую среду и снижение выбросов вредных веществ.
Использование метода электрохимического разложения является эффективной и перспективной технологией получения аммиака, обеспечивая устойчивое развитие и снижение негативного влияния на окружающую среду.
Применение аммиака в промышленности

Производство удобрений: Аммиак является основным компонентом азотной удобрения, такого как аммиачная селитра, амфос и карбамид. Он обеспечивает растения необходимым азотом для роста и развития.
Производство пластмасс: Аммиак используется в производстве синтетических пластмасс, таких как полиамиды (нейлон) и полиуретаны. Он служит важным сырьем для создания прочных и легких материалов, используемых в различных отраслях промышленности.
Текстильная промышленность: В процессе окраски и обработки текстильных материалов аммиак используется в качестве регулирующего агента и растворителя. Он способствует получению ярких и стойких красок на ткани и обеспечивает их обработку для улучшения качества и долговечности.
Охлаждающее средство: Аммиак широко используется в промышленности как охлаждающее средство. Он используется в холодильных системах, кондиционерах, холодильниках и других системах, где требуется низкая температура.
Производство взрывчатых веществ: В некоторых отраслях промышленности аммиак используется для производства взрывчатых веществ, таких как тротил и азоттрихлорид. Он является важным компонентом при создании взрывов и взрывной атмосферы в контролируемых условиях.
Это лишь некоторые примеры применения аммиака в промышленности. Его широкий спектр применения и химические свойства делают его одним из ключевых веществ для различных отраслей и процессов, необходимых для нашей современной промышленности.