Определение выпадения осадка по произведению растворимости является одним из ключевых методов химического анализа. Растворимость вещества определяет, насколько оно может раствориться в данном растворителе при определенной температуре. Если произведение растворимости (или произведение растворимости-брауна) для данных ионов превышает значение, указанное в таблице растворимости, то осадок образуется.
Произведение растворимости рассчитывается путем умножения концентраций всех ионов в растворе между собой. Для этого необходимо знать ионный состав вещества, его растворимость и ионный состав раствора. Значения концентраций ионов в растворе можно найти в таблице стандартного состояния и использовать их для рассчета произведения растворимости.
Если произведение растворимости превышает значение, указанное в таблице растворимости, то раствор ненасыщенный и осадок будет выпадать из раствора. Этот метод позволяет определить, какие вещества могут быть использованы для осаждения заданного иона или, наоборот, какие ионы могут образовать осадок при взаимодействии с заданным растворителем.
Как определить осадок в произведении растворимости?
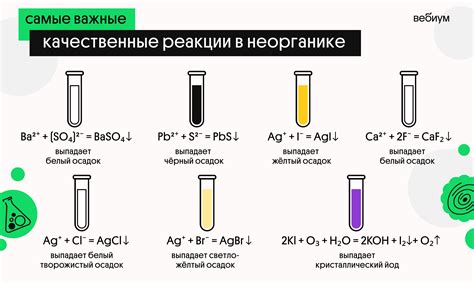
Осадок в произведении растворимости можно определить с помощью простого эксперимента. Возьмите некоторое количество вещества и растворите его в определенном количестве растворителя. Затем добавьте к раствору небольшое количество другого вещества и тщательно перемешайте.
Если после перемешивания образуется осадок – это означает, что произошло образование нерастворимого соединения. Осадок может иметь различную форму и цвет, что зависит от химических свойств веществ и условий эксперимента.
Чтобы подтвердить наличие осадка, можно провести также наблюдение за изменением цвета или прозрачности раствора. Если раствор изменил свой цвет или стал мутным, вероятно, в нем образовался осадок.
Однако стоит отметить, что не все осадки могут быть наглядно видны невооруженным глазом. Некоторые микроскопические осадки могут быть обнаружены только с использованием специальных приборов или методов анализа.
Таким образом, определить осадок в произведении растворимости можно с помощью наблюдения за появлением нерастворимого вещества в растворе и изменением его свойств. Этот метод является одним из основных способов определения произведения растворимости и позволяет оценить, насколько вещество может растворяться в данном растворителе.
Растворимость и осадки

Изменение условий растворения может происходить вследствие:
- Изменения температуры.
- Изменения концентрации раствора.
- Изменения рН раствора.
- Введения в раствор другого реагента, влияющего на процесс растворения.
Осадки могут быть обратимыми и необратимыми. В случае обратимых осадков, когда изменяются условия растворения, осадок может раствориться снова. Необратимые осадки не растворяются при изменении условий и остаются в твердом состоянии.
Для определения, выпадет ли осадок при произведении растворимости веществ, необходимо знать соответствующие значения растворимостей для каждого вещества и составить таблицу сравнения. Если произведение растворимостей веществ, входящих в реакцию, меньше или равно произведению растворимостей образующихся при реакции веществ, то осадок образуется и выпадает из раствора.
| Вещество | Растворимость |
|---|---|
| Вещество 1 | Значение растворимости 1 |
| Вещество 2 | Значение растворимости 2 |
| ... | ... |
| Вещество N | Значение растворимости N |
Если у вас есть значения растворимостей веществ и вы хотите определить, будет ли образовываться осадок при их смешивании, просто подставьте эти значения в таблицу и выполните сравнение произведений. Если произведение растворимостей веществ меньше или равно произведению растворимостей образующихся при реакции веществ, то осадок выпадет из раствора.
Экспериментальные методы определения осадков

Определение наличия или отсутствия осадков, образующихся при взаимодействии растворов, может быть осуществлено с использованием различных экспериментальных методов. Вот некоторые из них:
- Метод наблюдения
- Метод микроскопии
- Метод фильтрации
- Метод анализа химической реакции
Суть метода заключается в наблюдении непосредственно за образованием осадка при смешении двух растворов. Этот метод подразумевает визуальную оценку: образуется ли осадок или нет.
Данный метод позволяет определить наличие осадка или его тип с использованием микроскопа. Образец раствора помещается на предметное стекло и производится его подробное изучение при помощи микроскопа.
Этот метод основан на применении фильтрации для разделения осадка от оставшегося раствора. Осадок остается на фильтре, а раствор проходит через него. Далее осадок можно изучить под микроскопом или провести дополнительные анализы.
Суть данного метода заключается в изучении реакции, которая происходит при взаимодействии двух растворов. Образующийся осадок может быть обнаружен с помощью изменения окраски, образования газа или других видимых следов реакции.
Эти методы позволяют провести качественную оценку наличия или отсутствия осадков в растворах и определить их тип.
Анализ изменения цвета раствора
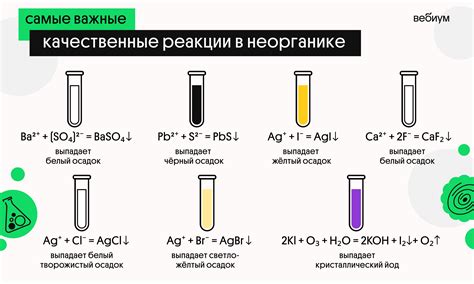
Для проведения анализа изменения цвета раствора необходимо:
- Подготовить раствор и заранее установить его цвет.
- После определенного времени наблюдения оценить изменение цвета раствора.
Изменение цвета раствора может говорить о нескольких вещах:
- Если раствор изначально был прозрачным, а стал мутным, это может указывать на образование осадка.
- Если раствор имел определенный цвет, а стал бесцветным или иной цвет, это может указывать на окисление или связывание определенных соединений.
- Если в результате реакции образовался новый соединение, которое имеет другой цвет, это может быть признаком того, что осадок выпал.
Важным моментом является сравнение цвета раствора после реакции с изначальным цветом. Для этого необходимо использовать справочные данные или сравнивать с контрольными пробами. Это позволит определить, произошло ли изменение цвета раствора и какое именно.
Добавление реактивов для обнаружения осадка
Реактивы могут быть использованы для определения наличия или отсутствия осадка в растворе. Для этого необходимо добавить соответствующие реагенты и проанализировать полученные результаты.
Перед добавлением реактивов необходимо установить цвет и прозрачность раствора. Это позволяет определить, что произошла реакция с реагентами.
Основные реактивы для обнаружения осадка включают следующие:
| Реагент | Инструкции по использованию |
|---|---|
| Аммиак (NH3) | Добавьте несколько капель аммиака в раствор и взболтайте. Наблюдайте визуальные изменения цвета или образование осадка. |
| Щавелевая кислота (C2H2O4) | Добавьте несколько капель щавелевой кислоты в раствор и аккуратно встряхните. Если образуется осадок, это может указывать на наличие кальция, свинца или оксалатов. |
| Хлорид бария (BaCl2) | Добавьте несколько капель хлорида бария в раствор и аккуратно встряхните. Если возникнет облачность или белый осадок, это может указывать на наличие сульфата или фосфата. |
Данные реактивы являются лишь примером того, какие реагенты можно использовать для обнаружения осадка. Важно учитывать химические свойства и особенности реагентов для правильного анализа растворов на наличие или отсутствие осадка.
Различия между осадками в зависимости от ионов

Осадки, образующиеся при произведении растворимости, могут значительно отличаться в зависимости от типа ионов, которые присутствуют в растворе. Различия в осадках определяются их химическим составом, структурой и физическими свойствами.
Некоторые осадки образуются при реакции двух или более растворов, содержащих разные ионы. Такие осадки называются двойными ионными осадками. В таблице ниже приведены примеры различных осадков, образующихся в зависимости от сочетания ионов:
| Ионы | Осадки |
|---|---|
| Ag+ и Cl- | AgCl (хлорид серебра) |
| Pb2+ и SO42- | PbSO4 (сульфат свинца) |
| Ca2+ и CO32- | CaCO3 (карбонат кальция) |
Кроме двойных ионных осадков, существуют также осадки, образующиеся при реакциях между одиночными ионами. Например, гидроксид натрия (NaOH) и гидроксид алюминия (Al(OH)3) образуются при реакции натрия и алюминия соответственно. Одиночные ионные осадки обычно имеют различную структуру и могут обладать разными свойствами.
Важно отметить, что каждый осадок имеет свою химическую формулу и свойства, которые могут сильно отличаться от других осадков. Поэтому при определении выпадения осадка по произведению растворимости необходимо учитывать состав реагентов и ионов, а также производить соответствующие измерения и анализы.
| Дата | Произведение растворимости | Наблюдаемый результат |
|---|---|---|
| 10.10.2022 | 0.5 г/л * 10 л = 5 г | Осадок не образуется |
| 12.10.2022 | 2 г/л * 5 л = 10 г | Образуется осадок |
| 15.10.2022 | 1 г/л * 8 л = 8 г | Осадок не образуется |