Масса раствора – важная характеристика, которая позволяет определить количество растворенного вещества в данном растворе. Точное знание массы раствора является основой для проведения экспериментов и расчетов в химии или физике. Однако, не всегда масса раствора находится непосредственно в измерительных приборах, а только его объем. В таких случаях, необходимо знать принципы расчета массы раствора по его объему.
Определение массы раствора по его объему является довольно простым процессом, основанным на простых математических формулах. В основе лежит понятие концентрации раствора – это отношение массы растворенного вещества к его объему. Для расчета массы раствора нам необходимо знать концентрацию, а также объем раствора.
Допустим, у нас есть раствор, объем которого измерен с помощью измерительного прибора, например, градуированного цилиндра. Пусть в этом растворе концентрация равна 10 г/л, а объем составляет 200 мл. Для определения массы раствора необходимо воспользоваться следующей формулой: масса = концентрация × объем. В нашем случае, масса раствора равна 10 г/л × 200 мл = 2000 г, или 2 кг.
Что такое масса раствора и как ее определить?

Определение массы раствора является существенным шагом для понимания его свойств и связанных с ним процессов. Существует несколько способов определения массы раствора.
Первый способ основан на измерении массы раствора непосредственно. Для этого необходимо взвесить пустой сосуд и затем добавить в него определенный объем раствора. Затем взвесить полученный сосуд с раствором. Разность масс до и после добавления раствора будет являться массой раствора.
Второй способ заключается в определении массы раствора на основе его концентрации и объема. Для этого нужно знать процентное содержание растворенного вещества (концентрацию) и объем раствора. После этого можно использовать формулу, которая позволяет вычислить массу раствора: масса = концентрация × объем.
Таким образом, определение массы раствора требует проведения измерений и использования математических формул. Правильное определение массы раствора является важным этапом для проведения более глубоких исследований в области химии и физики.
Что такое масса раствора?

Масса раствора зависит от концентрации растворенного вещества и его плотности. Концентрация обозначает количество растворенного вещества, приходящееся на единицу объема раствора. Плотность же – это масса раствора, приходящаяся на единицу его объема.
Зная объем и концентрацию раствора, можно легко определить его массу. Для этого необходимо умножить объем раствора на его плотность.
Масса раствора имеет большое значение в химии и физике, так как она позволяет определить количество вещества, участвующего в реакциях или процессах с данной средой. Благодаря этому параметру становится возможным проведение точных расчетов и определение физических и химических свойств растворов.
Чем отличается масса раствора от объема?

Масса раствора - это общая масса всех веществ, находящихся в растворе. Она измеряется в граммах или килограммах. Масса раствора может быть определена путем взвешивания сосуда с раствором перед и после растворения вещества в нем.
Объем же - это пространство, занимаемое раствором. Он измеряется в литрах или миллилитрах. Объем раствора можно измерить с помощью мерного цилиндра, пробирки или других сосудов, подходящих для данного раствора.
Несмотря на то, что масса и объем раствора разные величины, они тесно связаны между собой. Масса раствора зависит от концентрации растворенных веществ в растворе, а объем может изменяться в зависимости от температуры и давления.
Важно отметить, что масса раствора и объем раствора могут быть взаимосвязаны посредством плотности раствора:
Плотность раствора - это масса раствора, содержащаяся в единице объема раствора. Она вычисляется путем деления массы раствора на его объем. Плотность раствора может использоваться для определения массы раствора при известном объеме и наоборот.
Таким образом, масса раствора и объем - это важные характеристики растворов, которые помогают определить его состав и свойства. Знание различий между массой и объемом раствора позволяет сделать правильные расчеты и провести анализ растворов в химических и других научных исследованиях.
Как определить массу раствора?

Плотность раствора определяется как отношение массы раствора к его объему. Обычно плотность измеряется в г/мл или кг/м³. Для расчета массы раствора по объему необходимо знать плотность раствора и его объем.
| Обозначение | Описание |
| М | Масса раствора |
| В | Объем раствора |
| П | Плотность раствора |
Формула для расчета массы раствора:
М = П * В
Например, если плотность раствора равна 1 г/мл, а объем раствора составляет 50 мл, то масса раствора будет равна:
М = 1 г/мл * 50 мл = 50 г
Таким образом, масса раствора составляет 50 г.
Необходимо отметить, что плотность раствора может зависеть от температуры и концентрации раствора. Поэтому при расчете массы раствора по объему важно принимать во внимание значения этих параметров.
Определение массы раствора по известному объему

Для определения массы раствора по известному объему необходимо знать концентрацию раствора. Концентрация раствора выражается в виде процентного содержания растворенного вещества в растворе или в виде молярной концентрации.
Для расчета массы раствора по известному объему и концентрации необходимо использовать следующую формулу:
| Формула расчета массы раствора: |
|---|
| Масса раствора (г) = Объем раствора (мл) * Концентрация раствора (%) |
Пример использования формулы:
Предположим, у нас есть раствор с объемом 500 мл и концентрацией 10%. Чтобы определить его массу, нужно умножить объем на концентрацию:
| Данные: | Решение: |
|---|---|
| Объем раствора (мл) | 500 |
| Концентрация раствора (%) | 10 |
| Масса раствора (г) | 500 * 10% = 50 г |
Таким образом, масса раствора равна 50 г.
Определение массы раствора с помощью плотности вещества
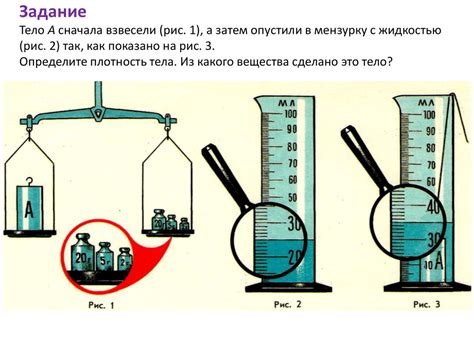
Для вычисления массы раствора с использованием плотности необходимо знать объем раствора и плотность вещества, которое растворяется. Формула для расчета массы раствора выглядит следующим образом:
Масса раствора = Объем раствора * Плотность вещества
Для примера, если у вас есть 100 мл раствора и известно, что плотность вещества составляет 1 г/мл, то масса этого раствора будет равна:
Масса раствора = 100 мл * 1 г/мл = 100 г
Таким образом, зная объем раствора и плотность вещества, вы можете определить массу раствора с помощью формулы, описанной выше.
Определение массы раствора неизвестного вещества
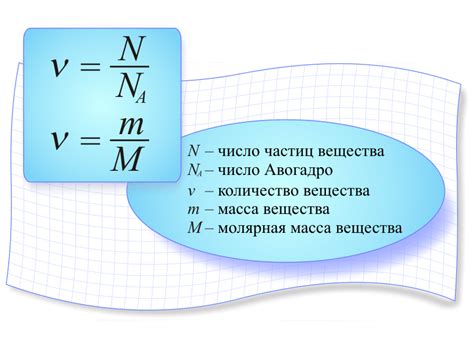
Шаги для определения массы раствора:
- Измерьте объем раствора с использованием градуированной пробирки или мерного цилиндра. Запишите полученное значение.
- Определите плотность раствора с помощью пикнометра или другого метода. Плотность может быть известна из ранее проведенных исследований или она может быть найдена в справочном материале.
- Умножьте объем раствора на плотность, чтобы получить массу раствора. Например, если объем раствора составляет 100 мл, а плотность 1 г/мл, то масса раствора будет равна 100 г.
Важно помнить, что для более точного определения массы раствора неизвестного вещества, необходимо использовать точные измерительные инструменты и проводить повторные измерения для усреднения результатов.
Определение массы раствора является важным этапом не только в лабораторных условиях, но также и в промышленных процессах, где точность определения массы может влиять на качество и эффективность производства.
Особенности определения массы раствора при изменении температуры
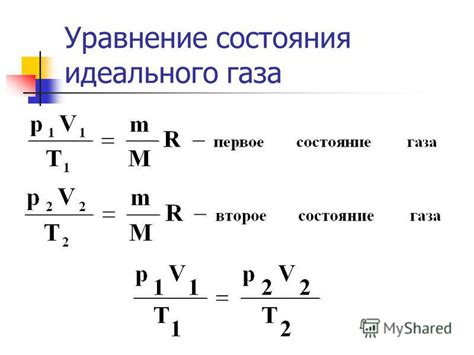
Изменение температуры может оказывать значительное влияние на массу раствора и, следовательно, на его концентрацию.
При повышении температуры растворность многих веществ увеличивается, что приводит к увеличению массы раствора. Это обусловлено тем, что при повышенной температуре частицы растворенного вещества обладают большей энергией, что способствует их более интенсивному перемешиванию с растворителем.
Однако, существуют и такие вещества, растворимость которых уменьшается с повышением температуры. В этом случае, при повышении температуры, наблюдается уменьшение массы раствора, так как часть растворенного вещества выделяется в виде кристаллических осадков.
При определении массы раствора при изменении температуры, необходимо учитывать какое-либо возможное взаимодействие растворенного вещества с растворителем. Такие взаимодействия могут привести к химическим реакциям и изменению состава раствора. В этом случае лучше использовать другие методы и приборы для определения массы раствора, учитывающие химические изменения.
Существуют ли альтернативные методы определения массы раствора?

В процессе определения массы раствора по его объему существуют несколько альтернативных методов, которые могут быть использованы в различных ситуациях или при особых условиях.
Один из таких методов - использование плотности раствора. Плотность раствора может быть определена с помощью специального прибора, такого как ареометр или пикнометр. Зная плотность раствора и его объем, можно вычислить массу раствора при помощи формулы:
масса = плотность × объем
Другим альтернативным методом является использование концентрации раствора. Концентрация раствора определяется как количество растворенного вещества, выраженное в единицах массы или молярного количества, на единицу объема раствора. Зная концентрацию раствора и его объем, можно вычислить массу раствора при помощи формулы:
масса = концентрация × объем
Для определения концентрации раствора может использоваться метод титрования, когда с помощью реакции с известным объемом и концентрацией раствора определяется неизвестная концентрация раствора.
Таким образом, существуют различные методы определения массы раствора по его объему, из которых можно выбрать наиболее подходящий в зависимости от конкретной ситуации или требуемой точности результатов.